Etwa jede zweite Frau ist im Laufe ihres Lebens von einer Blasenentzündung betroffen, und viele leiden unter wiederkehrenden Harnwegsinfektionen. Blaseninfektionen sind nicht nur schmerzhaft und potenziell gefährlich, sondern stellen auch ein erhebliches Dilemma für Ärzte dar. Angesichts der weit verbreiteten Antibiotikaresistenz bei Harnwegsinfektionen, die kontinuierlich zunimmt, sind Ärzte oft gezwungen, Antibiotika blind zu verschreiben, ohne deren Wirksamkeit gegen den Erreger, der die Infektion verursacht, zu kennen. Dies liegt daran, dass es mehrere Tage dauert, einen spezifischen Erreger mithilfe konventioneller Diagnostikverfahren zu identifizieren.
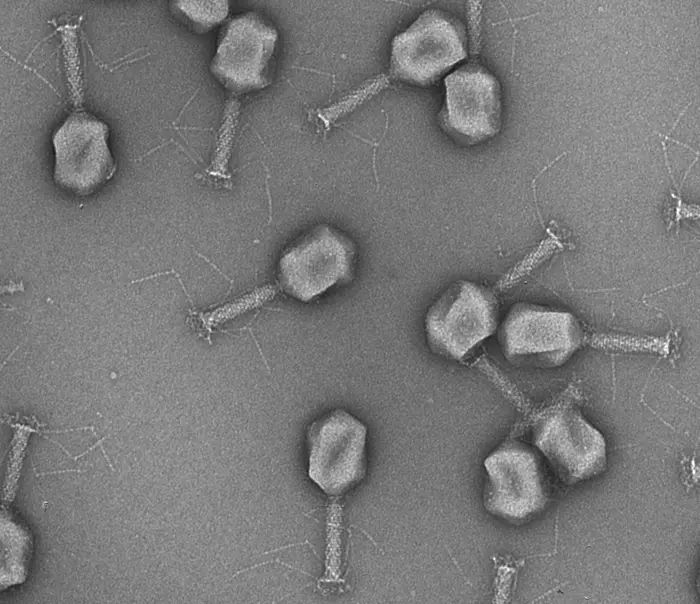
Forscherinnen und Forscher der ETH Zürich haben in Zusammenarbeit mit dem Balgrist Universitätsspital nun einen Schnelltest entwickelt, der die natürlichen Feinde von Bakterien, Bakteriophagen, einsetzt. Die Forschenden haben die Phagen auch genetisch modifiziert, um sie effizienter bei der Zerstörung der krankheitserregenden Bakterien zu machen.
Schnelle und genaue Diagnose möglich
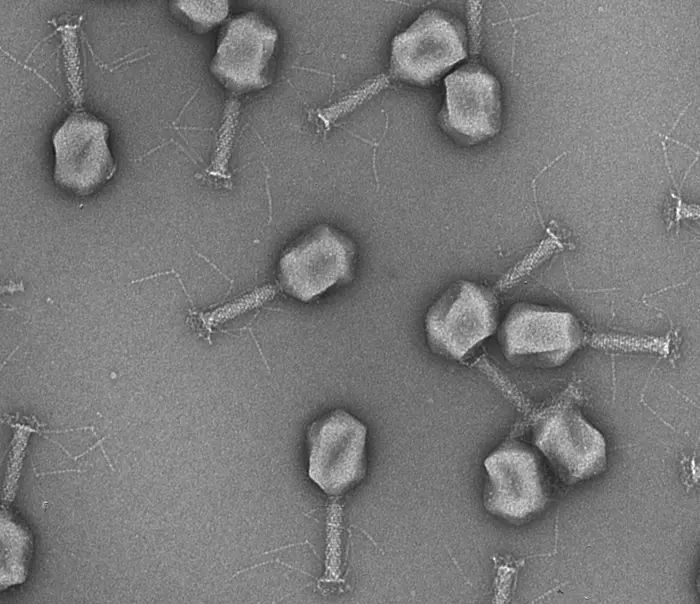
Bakteriophagen sind hochspezialisierte Viren. Jede Art von Bakteriophagen infiziert nur einen bestimmten Typ oder Stamm von Bakterien. Wissenschaftlerinnen und Wissenschaftler der ETH Zürich aus der Forschungsgruppe für Lebensmittel-Mikrobiologie unter der Leitung von Professor Martin Loessner nutzen nun diese einzigartige Eigenschaft. Der erste Schritt bestand darin, die Bakteriophagen zu identifizieren, die gegen die drei Hauptarten von Bakterien wirksam sind, die für Harnwegsinfektionen verantwortlich sind, nämlich Escherichia coli, Klebsiella und Enterokokken. Diese natürlichen Bakteriophagen wurden dann so modifiziert, dass die Bakterien, die sie erkennen und infizieren, ein leicht messbares Lichtsignal erzeugen.
Mit dieser Methode konnten die Forscherinnen und Forscher die krankheitserregenden Bakterien zuverlässig direkt aus einer Urinprobe in weniger als vier Stunden nachweisen. In Zukunft könnte die Methode es ermöglichen, unmittelbar nach der Diagnose ein geeignetes Antibiotikum zu verschreiben und damit die Resistenzentwicklung zu minimieren und das Antibiotika-Management zu verbessern.
Die Methode hat auch einen weiteren Vorteil: Sie ermöglicht es Ärztinnen und Ärzten vorherzusagen, bei welchen Patientinnen und Patienten eine maßgeschneiderte Bakteriophagen-Therapie besonders gut anschlagen wird, da die Stärke des im Test erzeugten Lichtsignals bereits darauf hinweist, wie effizient die Bakteriophagen in der Bekämpfung des Bakteriums sind – je mehr das Probenmaterial leuchtet, desto besser wird das Bakterium auf die Therapie ansprechen.
Viren vs. Blaseninfektionen: Mit Bacterioinen doppelt wirksam
Phagentherapien werden seit über 100 Jahren eingesetzt, gerieten jedoch in Vergessenheit in den westlichen industrialisierten Ländern mit der Entdeckung von Penicillin. Angesichts zunehmender Antibiotikaresistenz erleben sie derzeit eine Wiedergeburt. Sie haben auch den entscheidenden Vorteil, nur ein einzelnes Zielbakterium anzugreifen, ähnlich wie ein Scharfschütze.
Allerdings haben bisherige therapeutische Ansätze ein Problem: „Phagen haben kein Interesse daran, ihren Wirt, das pathogene Bakterium, vollständig abzutöten“, erklärt der ETH-Forscher Samuel Kilcher, einer der beiden Hauptautoren der Studie. Um die Wirksamkeit der Phagen zu erhöhen, haben die Forscher sie genetisch modifiziert. Die modifizierten Phagen produzieren nicht nur neue Phagen innerhalb des infizierten Wirtsbakteriums, sondern auch Bakteriocine. Sobald sie freigesetzt werden, sind diese bakterientötenden Proteine besonders wirksam gegen Bakterienstämme, die Teile ihrer Oberfläche so verändert haben, dass die Phagen sie nicht mehr erkennen. Dieser doppelte Angriff macht die Behandlung effektiver.
Ausblick: Vom Labor in die Klinik
In Einzelfällen, wie der kürzlichen Rettung eines Lungenpatienten im Universitätsspital Genf, wurden Phagentherapien erfolgreich experimentell eingesetzt. „Weltweit laufen auch viele akademische und kommerzielle klinische Studien, die systematisch das Potenzial natürlicher und genetisch optimierter Phagen untersuchen“, sagt Matthew Dunne, einer der letzten Autoren der Studie. Dennoch ist es ein langer Weg, bevor solche Therapien in westlichen Ländern breiter angewendet werden können. Neben umfangreichen klinischen Studien wären auch regulatorische Anpassungen sinnvoll, unter Berücksichtigung der Tatsache, dass Phagen biologische Einheiten sind, die gemeinsam mit ihren bakteriellen Wirten mitevolvieren, d.h. ständig im Wandel sind.
Die vorliegende Studie ist ein Proof of Concept. Als Nächstes werden die Forscher der ETH Zürich gemeinsam mit ihren Partnern vom Universitätsspital Balgrist die Wirksamkeit der neuen Phagentherapie in einer klinischen Studie mit ausgewählten Patienten testen
Quelle: EurekAlert (zur Originalpressemitteilung)
Disclaimer: Der Text wurde mit KI-Unterstützung erstellt.