In der Behandlung nicht-melanozytärer Hauttumoren ist die moderne Strahlentherapie eine effektive, funktionserhaltende Alternative zur Operation mit guten kosmetischen Ergebnissen. Bei niedrigen Nebenwirkungen ist sie insbesondere bei älteren Patienten oder anspruchsvollen Lokalisationen eine gute Option.
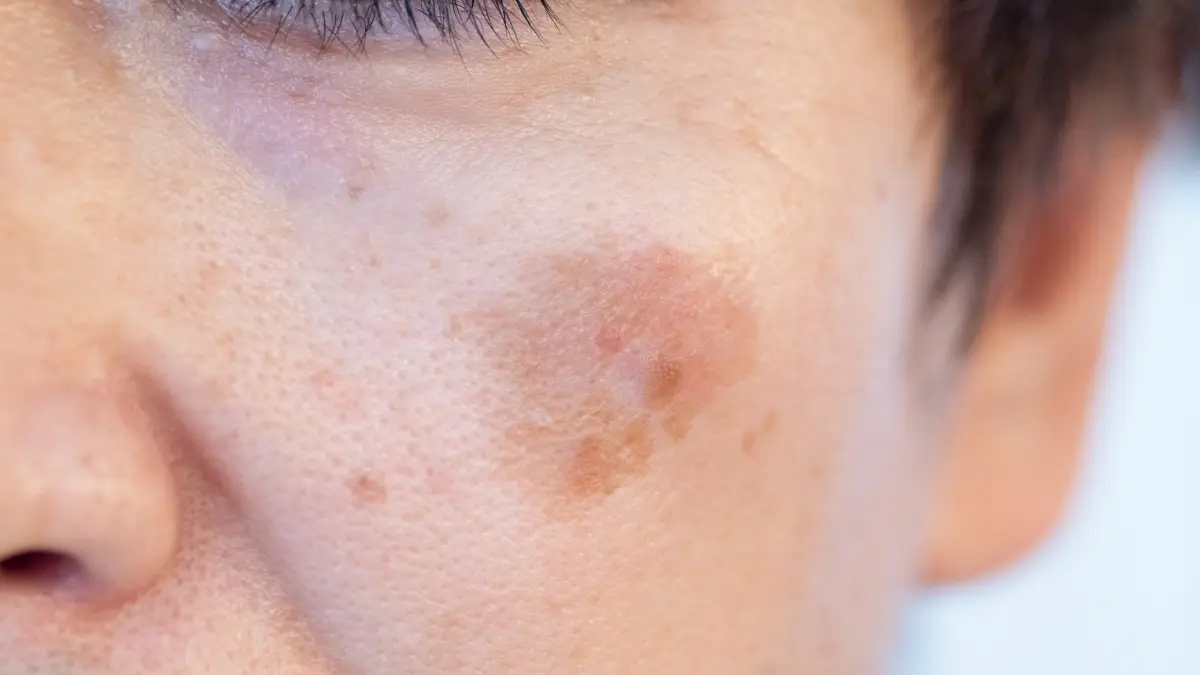
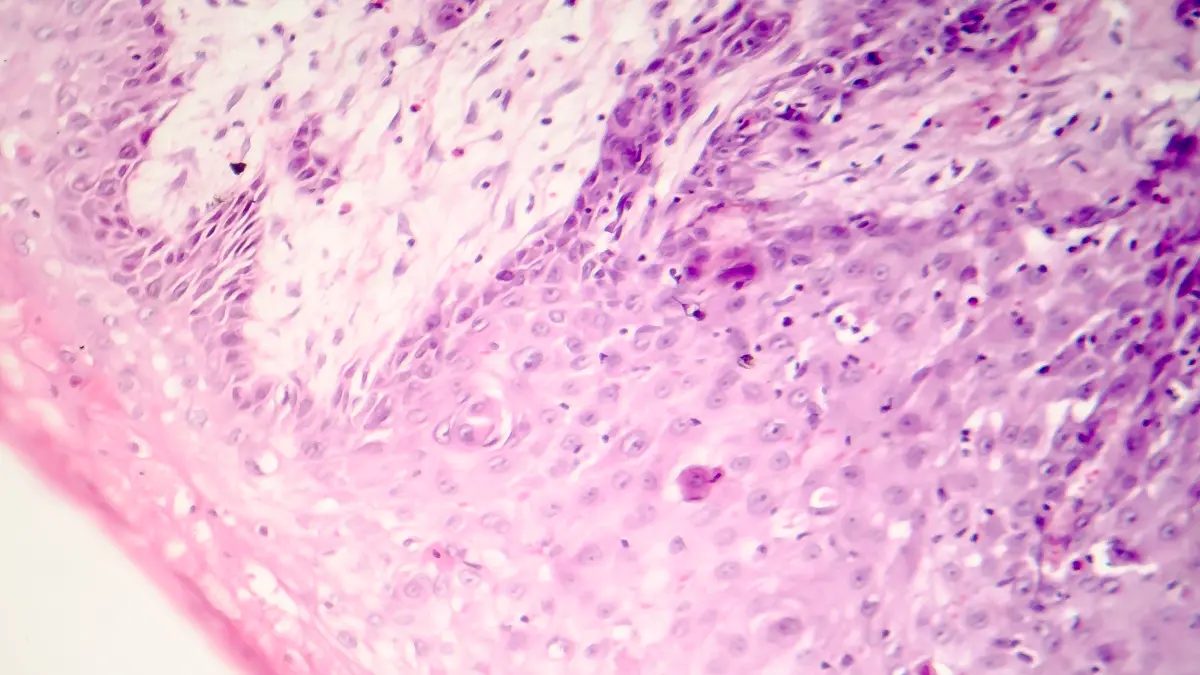
Nicht-melanozytäre Hauttumoren (Non-Melanoma-Skin-Cancer, NMSC, im wesentlichen Basalzellkarzinome oder kutane Plattenepithelkarzinome) sind die häufigste maligne Erkrankung überhaupt. Besonders die hellhäutige Population hat ein signifikantes Risiko NMSC zu entwickeln, insbesondere in Regionen hoher UV-Exposition und an sonnenexponierten Lokalisationen wie der Kopf-Hals-Region. Weltweit sind steigende Inzidenzen zu verzeichnen, weshalb die Versorgung der Patienten in Zukunft eine zunehmende Herausforderung darstellt.
Obwohl nicht-melanozytäre Hauttumoren häufige Erkrankungen sind, gibt es nur wenige prospektiv randomisierte Studien, die z. B. Strahlentherapie mit einer Operation vergleichen.
Daher haben sich Behandlungskonzepte oft auf empirischer Basis entwickelt1,2. Die Strahlentherapie ist neben der primären operativen Behandlung ein wichtiger Bestandteil im Management von NMSC und ist in manchen klinischen Situationen sogar als Erstlinientherapie einer Operation überlegen. Die Rolle der Strahlentherapie umfasst dabei sowohl definitive, adjuvante als auch palliative Therapieoptionen.
Radiotherapie vs. Operation als definitive Therapie
Die chirurgische Sanierung ist üblicherweise die Therapie der ersten Wahl bei NMSC. Die Strahlentherapie stellt jedoch eine effektive, nicht-invasive Option mit sehr hohen Ansprechraten von über 90 % im definitiven Setting dar.
Gerade bei steigenden Inzidenzen und einer immer älter werdenden Gesellschaft gewinnt sie zunehmend an Bedeutung. Denn vor allem bei älteren Patienten, Patienten mit Komorbiditäten oder geringer Lebenserwartung sowie bei schwer zu operierenden Tumoren bietet die Strahlentherapie einige Vorteile. Insbesondere bei Kontraindikationen für eine chirurgische Sanierung (z. B. Blutgerinnungsstörungen) oder im Fall von Tumorlokalisationen, bei denen eine Operation große negative Auswirkungen auf Funktion oder Kosmetik hätte, sollte eine Strahlentherapie in Betracht gezogen werden. In Regionen, in denen die vorgeschriebenen Sicherheitsabstände bei einer Operation nicht eingehalten werden könnten, ohne einen Substanzdefekt zu verursachen, wie beim Auge (medialer Augenwinkel, Augenlider), Nase, Ohr, Lippen oder der Kopfhaut, ist der Radiotherapie der Vorzug zu geben3,4.
Auch bei lokal fortgeschrittenen Hauttumoren (T4), die z. B. Knochen, Muskeln oder Nerven infiltrieren, kann die definitive Radiotherapie eine kurative Option sein. Die Kontrollraten bei diesen großen Tumoren liegen mit 80 % deutlich unter den Ergebnissen von unkomplizierten, kleineren Tumoren, die Behandlung mit einer Radiatio kann jedoch häufig eine Tumorverkleinerung bzw. ein Verdrängen des Tumors aus kritischen Strukturen bewirken. Somit wird in vielen Fällen eine Salvage-Operation ermöglicht.
Einige Faktoren sprechen gegen eine Radiotherapie. Hierzu zählen z. B. junges Alter, eine vorangegangene Radiotherapie oder genetisch bedingte Hauttumoren (Gorin- Goltz-Syndrom, Li-Fraumeni-Syndrom, Ataxia teleangiectasia)2. In diesen Fällen sollte eine chirurgische Sanierung angestrebt werden.
Adjuvante Radiotherapie
Ungefähr 5 % der Patienten mit NMSC haben Risikofaktoren für das Auftreten von Rezidiven nach Operation sowie für die Entwicklung von Lymphknoten- oder Fernmetastasen. Zu diesen Risikofaktoren zählen Tumorlokalisation an Ohren oder Lippen, schlechte histologische Differenzierung, perineurale Invasion und patientenbezogene Faktoren wie Immunsuppression5.
Durch eine adjuvante Radiotherapie kann sowohl die Lokalkontrolle als auch das metastasenfreie Überleben verbessert werden.1
Risikofaktoren, die für eine postoperative Radiotherapie sprechen6:
Klinische oder radiologische perineurale Invasion: Perineurale Invasion geht mit einem höheren Rezidivrisiko und einer schlechteren Prognose einher, jedoch bleibt die perineurale Invasion oftmals nicht dokumentiert.
Knappe oder positive Schnittränder ohne Möglichkeit einer Nachresektion
Rezidivtumoren nach einer vorangegangenen R0-Resektion
Große Tumoren (T3–T4): Tumoren > 2 cm sind mit einem signifikant höheren Lokalrezidivrisiko verbunden. Bei Tumoren > 6 cm wurde ein Risiko von 16 % für die Entwicklung von Metastasen festgestellt7.
Desmoplastische oder infiltrative kutane Plattenepithelkarzinome bei immunsupprimierten Patienten: Immunsupprimierte Patienten haben sowohl ein höheres Risiko für die Entwicklung eines nicht-melanozytären Hautkrebses als auch ein höheres Risiko für einen schlechteren Verlauf. Manyam et al. zeigten in einer Kohorte von 205 Patienten, welche bei kutanem Plattenepithelkarzinom eine Operation und adjuvante Radiotherapie erhielten, ein deutlich schlechteres Outcome in der Gruppe der immunsupprimierten Patienten im Vergleich zu den immunkompetenten Patienten mit einem progressionsfreien Überleben von 38,7 % vs. 71,6 % nach 2 Jahren8.
Strahlentherapie im palliativen Setting
Im palliativen Setting hat die Radiotherapie das Potenzial, krankheitsbezogene Symptome wie Schmerzen, Blutung oder Ulzeration zu lindern. Insgesamt sollte in der Palliativsituation jedoch beachtet werden, dass die Lebensqualität der Patienten im Vordergrund steht und daher eher hypofraktionierte Fraktionierungsschemata (kürzere Behandlungszeit mit höheren Einzeldosen) bevorzugt werden sollten2. In der Literatur finden sich unterschiedliche Fraktionierungsschemata, Barnes et al. untersuchten 24 Gy in 3 Fraktionen und konnten damit in 61 % eine Symptomkontrolle erreichen9. Aber auch wöchentliche hypofraktionierte Konzepte mit 56–64 Gy in 7–8 Fraktionen konnten als gut verträgliche und symptomkontrollierende Fraktionierungen gezeigt werden. Nach 12 Wochen kam es bei 65 % zu einem kompletten bzw. bei 30 % zu einem partiellen Ansprechen10.
Technische Besonderheiten in der Radiotherapie des NMSC
Um eine adäquate Behandlung des NMSC durch eine Radiotherapie zu gewährleisten, sollten mehrere Bestrahlungsarten bzw. -techniken zur Verfügung stehen. So werden für die Bestrahlung im oberflächlichen Hautbereich eine Röntgenschwachbestrahlung und/oder Elektronenbestrahlung sowie für die Behandlung von tiefer gelegenen Strukturen wie den Lymphknoten ein Linearbeschleuniger mit hochenergetischen Strahlen benötigt. In Sonderfällen ist sogar eine Brachytherapie, die meist nur in hochspezialisierten Zentren angeboten wird, notwendig. Aufgrund der komplexen und teuren Ausstattungserfordernisse kann die Behandlung von NMSC oft nur in dezidierten Zentren angeboten werden. Somit ist diese Therapieoption in vielen Gebieten unterrepräsentiert bzw. nur limitiert verfügbar. Um den Patienten trotzdem eine optimale Therapie anbieten zu können, sollte zumindest eine interdisziplinäre – eventuell digitale – Vorstellung erfolgen. Falls notwendig, können die Patienten anschließend an ein Zentrum vermittelt werden.
Je nach angewandter Technik dauert eine einzelne Bestrahlung nur wenige Minuten und kann grundsätzlich ambulant durchgeführt werden. Das Bestrahlungsgebiet wird durch die Größe und Lokalisation beeinflusst. Typischerweise wird ein Sicherheitsabstand wie auch bei Operationen von ca. 0,5–2 cm je nach Tumorhistologie und -ausbreitung gewählt. Im Gegensatz zu einer Operation können die Sicherheitsabstände trotz Schwierigkeiten an anatomischen Grenzen gut eingehalten werden.
Abhängig vom Alter und Anfahrtsweg der Patienten sowie den Tumoreigenschaften existieren verschiedene Strahlentherapiekonzepte bezüglich Dosis und Dauer, die zwischen 5 und 30 Bestrahlungstagen variieren können.
Bei älteren Patienten oder reduziertem Allgemeinzustand sollte die Behandlungszeit möglichst verkürzt werden. So bieten hypofraktionierte Bestrahlungsschemata eine effektive Option mit tolerablem Nebenwirkungsprofil1. Marriappan et al. zeigten eine lokale Kontrollrate von 95 % bei einem wöchentlichen Schema mit einer Einzeldosis von 6 Gy in sieben Fraktionen11.
Sonderform: Lidbestrahlung
Einen besonderen Stellenwert bei der Behandlung von NMSC nimmt die Radiatio von Tumoren im periokularen Bereich ein. Ungefähr 5 % der NMSC im Kopf-Hals-Bereich treten im Bereich der Augenlider oder -winkel auf, die die Funktion des Auges, den Visus und die Lebensqualität des Patienten stark beeinträchtigen können. Durch den Schutz der Augenbraue vor UV-Strahlung treten Tumoren häufiger im Bereich des Unterlides (48 %) oder im medialen Augenwinkel (27 %) auf.
Eine Operation ist im Bereich der Augenlider und -winkel oft aufgrund der zu erwartenden Funktionseinbußen nicht gut möglich bzw. birgt sie durch die Entwicklung eines Lagophthalmus mit Hornhauteinschmelzung letztendlich ophthalmologische Risiken bis hin zur Enukleation. Die Strahlentherapie kann die funktionelle Anatomie der Augenlider und dadurch meistens auch den Visus besser erhalten12. Jedoch ist speziell diese Form der Bestrahlungen in Bezug auf Technik und Durchführung herausfordernd. Um den Bulbus bestmöglich zu schonen und Nebenwirkungen so gering wie möglich zu halten, wird beispielsweise bei jeder Bestrahlung eine Augenschale aus Wolfram eingesetzt.
Nebenwirkungen
Zu den frühen Nebenwirkungen einer Strahlentherapie zählen Hautreaktionen, die von einer Rötung bis hin zu Epitheliolysen reichen können. Unter entsprechender Lokalpflege (Wundsalben, Antibiotika, Steroide) heilen diese in den meisten Fällen rasch wieder ab. Zu den Spätreaktionen zählen Hypopigmentierung, Alopezie, Teleangiektasien, Fibrose und epidermale Atrophie.
Vor allem bei jungen Patienten ist ein Augenmerk auf mögliche langfristige Nebenwirkungen wichtig. Die Wahrscheinlichkeit, im späteren Verlauf (10–15 Jahre) einen strahleninduzierten Tumor – meistens Sarkome – zu entwickeln, ist sehr gering und wird auf 1:1.000 geschätzt11. Mit modernen Techniken und kleinen Bestrahlungsfeldern ist dieses Risiko in der Realität vermutlich noch geringer. Dennoch sollten Patienten im jüngeren Alter dahingehend aufgeklärt werden. Die Dosis pro Fraktion sollte zudem individuell optimiert werden, um ein besseres langfristiges kosmetisches und funktionelles Ergebnis zu erzielen.
Zusammenfassung
Die Strahlentherapie stellt bei nicht-melanozytären Hauttumoren eine effektive Alternative zur Operation dar. Durch die Strahlentherapie kann ein gutes kosmetisches Ergebnis erzielt und oftmals die Funktion erhalten werden. Insbesondere bei älteren Patienten oder ungünstigen Tumorlokalisationen wie beispielsweise dem Augenlid sollte aufgrund des günstigen Nebenwirkungsprofils die Bestrahlung in Betracht gezogen werden. Dabei kann diese Therapieoption sowohl im definitiven, adjuvanten oder auch palliativen Setting eingesetzt werden. Nach Einschätzung der Autorinnen ist die Strahlentherapie in der Behandlung von NMSC derzeit unterrepräsentiert. Zu den Herausforderungen zählt dabei insbesondere eine eingeschränkte Verfügbarkeit; in urbanen Regionen ist eine entsprechende Versorgungslage jedoch meist gegeben. Eine gute Kooperation zwischen Dermatologen und Radioonkologen bietet die entsprechende Basis, um eine bestmögliche, personalisierte Therapie zu ermöglichen.
Dr. med. Mercedes Hudelist-Venz, Dr. med. Cora Waldstein, Wien
Literatur:
- Veness MJ et al. Current Role of Radiotherapy in Non-melanoma Skin Cancer. Clin Oncol (R Coll Radiol) 2019; 31(11): 749–58.
- Benkhaled S et al. The State of the Art of Radiotherapy for Non-melanoma Skin Cancer: A Review of the Literature. Front Med (Lausanne) 2022; 9: 913269.
- Rong Y et al. Radiotherapy treatment for nonmelanoma skin cancer. Expert Rev Anticancer Ther 2015; 15(7): 765–76.
- Strom TJ et al. Harrison, Management of BCC and SCC of the Head and Neck. Cancer Control 2016; 23(3): 220–7.
- Caparrotti F et al. Localized Nonmelanoma Skin Cancer: Risk Factors of Post-surgical Relapse and Role of Postoperative Radiotherapy. Curr Treat Options Oncol 2020; 21(12): 97.
- Likhacheva A et al. Definitive and Postoperative Radiation Therapy for Basal and Squamous Cell Cancers of the Skin: Executive Summary of an American Society for Radiation Oncology Clinical Practice Guideline. Pract Radiat Oncol 2020; 10(1): 8–20.
- Thompson AK et al. Risk Factors for Cutaneous Squamous Cell Carcinoma Recurrence, Metastasis, and Disease-Specific Death: A Systematic Review and Meta-analysis. JAMA Dermatol 2016; 152(4): 419–28
- Manyam BV et al. A multi-institutional comparison of outcomes of immunosuppressed and immunocompetent patients treated with surgery and radiation therapy for cutaneous squamous cell carcinoma of the head and neck. Cancer 2017; 123(11): 2054–60
- Barnes EA et al. Palliative radiotherapy for non-melanoma skin cancer. Clin Oncol (R Coll Radiol) 2010; 22(10): 844–9
- De Felice F et al. Definitive weekly hypofractionated radiotherapy in cutaneous squamous cell carcinoma: response rates and outcomes in elderly patients unfit for surgery. Int J Dermatol 2022; 61(8): 911–15
- Marriappan L et al. Weekly radiotherapy for basal cell carcinoma in the frail and elderly. Br J Dermatol 2014; 171(5): 1237–9
Bildquelle: © Symfonia – stock.adobe.com