Christoph Stein-Thoeringer, Professor für Klinische Infektiologie und Translationale Mikrobiomforschung am Uniklinikum Tübingen, leitet das Forschungsprojekt ResCPa zur CAR-T-Zell-Therapie beim Pankreaskarzinom. Beteiligt sind die Unikliniken Freiburg, Heidelberg und Würzburg, das TUM Universitätsklinikum rechts der Isar, das Berlin Institute of Health at Charité (BIH), das Nationale Centrum für Tumorerkrankungen (NCT) Heidelberg sowie das Biotech-Unternehmen Miltenyi Biotec. Das Forschungsprojekt wird vom Bundesministerium für Bildung und Forschung (BMBF) mit knapp 10 Millionen EUR unterstützt.
Die CAR-T-Zelltherapie bei soliden Tumoren soll deshalb schwierig sein, weil es kaum geeignete tumorspezifische Zielantigene gibt. Mit CD318 wurde aber doch ein Pankreaskarzinom-spezifisches Zielantigen gefunden?
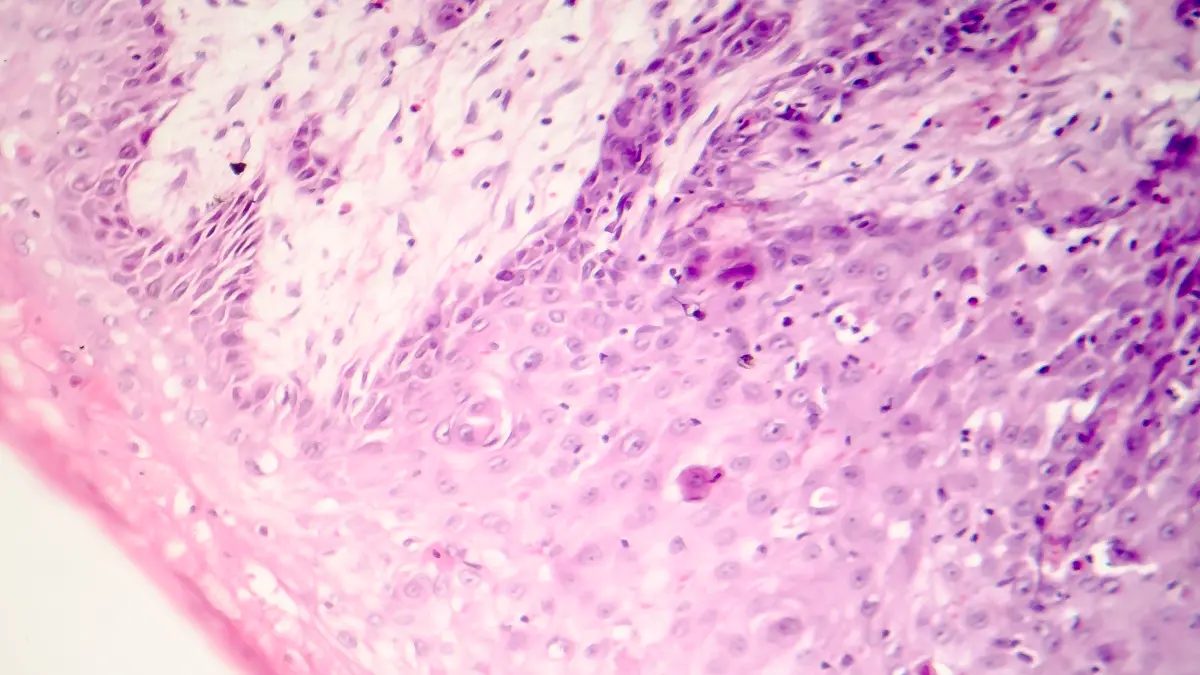
Stein-Thoeringer: CD318 ist auf Pankreaskarzinomzellen überexprimiert, kommt aber auch auf normalen Zellen vor. Hinsichtlich der Bindungsaffinität des CARs ist ein gewisses Feintuning möglich, um die Bindung an Zielstrukturen auf der Oberfläche von Tumorzellen zu erhöhen. Bei der Entwicklung der Produkte werden viele verschiedene Bindungsdomänen getestet. Der „Binder“ mit bestmöglicher Wirksamkeit bei gleichzeitig niedriger Toxizität wird dann verwendet. Hinsichtlich CD318 als Zielstruktur besitzen die von Miltenyi Biotec, unserem Industriepartner in ResCPa, entwickelten CARs eine sehr viel höhere Affinität zu Pankreaskarzinomzellen, so dass das Risiko von Toxizität laut den präklinischen Daten als gering einzuschätzen ist.
Wie ist man auf CD318 als Zielstruktur gestoßen?
Stein-Thoeringer: Wissenschaftler bei Miltenyi Biotec haben CD318 und zwei weitere Antigene als potenzielle Zielstrukturen bei Pankreaskrebs identifiziert [1]. Vorausgegangen war ein aufwendiger Prozess der präklinischen Strukturfindung. Wir haben uns aufgrund der überzeugenden Daten in vitro und im Tiermodell für CD318 als Zielstruktur entschieden. Am Tiermodell kann man nach Anwendung dieses CAR-T-Zellprodukts beobachten, wie Pankreastumoren schmelzen – und das bei geringer Toxizität. Wir können uns, wenn wir jetzt mit der klinischen Phase beginnen, auf ein sehr solides Fundament präklinischer Daten stützen.