Göttinger Forschende zeigen: Die Blockade zweier Signalwege tötet Krebszellen und aktiviert das Immunsystem. Ein neuartiger Therapieansatz könnte die Behandlung von Pankreaskrebs verbessern.
Bauchspeicheldrüsenkrebs, auch Pankreaskarzinom genannt, gehört zu den aggressivsten Tumorerkrankungen. Die Überlebenschancen sind trotz moderner Therapien nach wie vor sehr gering und viele Patient*innen entwickeln Resistenzen gegen die verfügbaren Behandlungen, weil sich die Tumorzellen durch Ausweichstrategien rasch anpassen. Forschende der Universitätsmedizin Göttingen (UMG), der Technischen Universität München (TUM), des Georg-Speyer-Hauses Frankfurt und der Charité – Universitätsmedizin Berlin haben nun gemeinsam einen neuartigen Therapieansatz entdeckt, der die Wirksamkeit der Behandlung deutlich verbessern könnte.
Unter der Leitung von Priv.-Doz. Dr. Matthias Wirth, Leiter der Arbeitsgruppe „Funktionelle Genomik und Therapieresistenz“, und Prof. Dr. Günter Schneider, Schwerpunktleiter Translationale Forschung, beide in der Klinik für Allgemein-, Viszeral- und Kinderchirurgie der UMG, sowie Prof. Dr. Ulrich Keller, Ärztlicher Direktor der Medizinischen Klinik mit Schwerpunkt Hämatologie, Onkologie und Tumorimmunologie der Charité – Universitätsmedizin Berlin, konnte das Forschungsteam zeigen, dass die gleichzeitige Blockade der beiden zellulären Signalwege PI3Kα/δ und SUMO Pankreaskrebszellen gezielt abtötet. In Tiermodellen führte diese Kombinationstherapie zu einer deutlichen Verringerung des Tumorwachstums und aktivierte zusätzlich das körpereigene Immunsystem, um die Krebszellen zu bekämpfen. Die Forschungsarbeiten wurden durch die Deutsche Forschungsgemeinschaft (DFG), die Deutsche Krebshilfe, Hector Stiftungen, Wilhelm Sander-Stiftung und dem Deutschen Konsortium für Translationale Krebsforschung (DKTK) unterstützt. Die Ergebnisse wurden in der Fachzeitschrift „Gastroenterology“ veröffentlicht.
„Unsere Arbeit zeigt, dass nur die gemeinsame Blockade beider Signalwege – PI3Kα/δ und SUMO – zur erfolgreichen Bekämpfung der Tumorzellen führt. Dies ist ein vielversprechender Ansatz für eine dringend benötigte neue Behandlungsstrategie“
Prof. Dr. Schneider, einer der drei Letztautoren der Studie
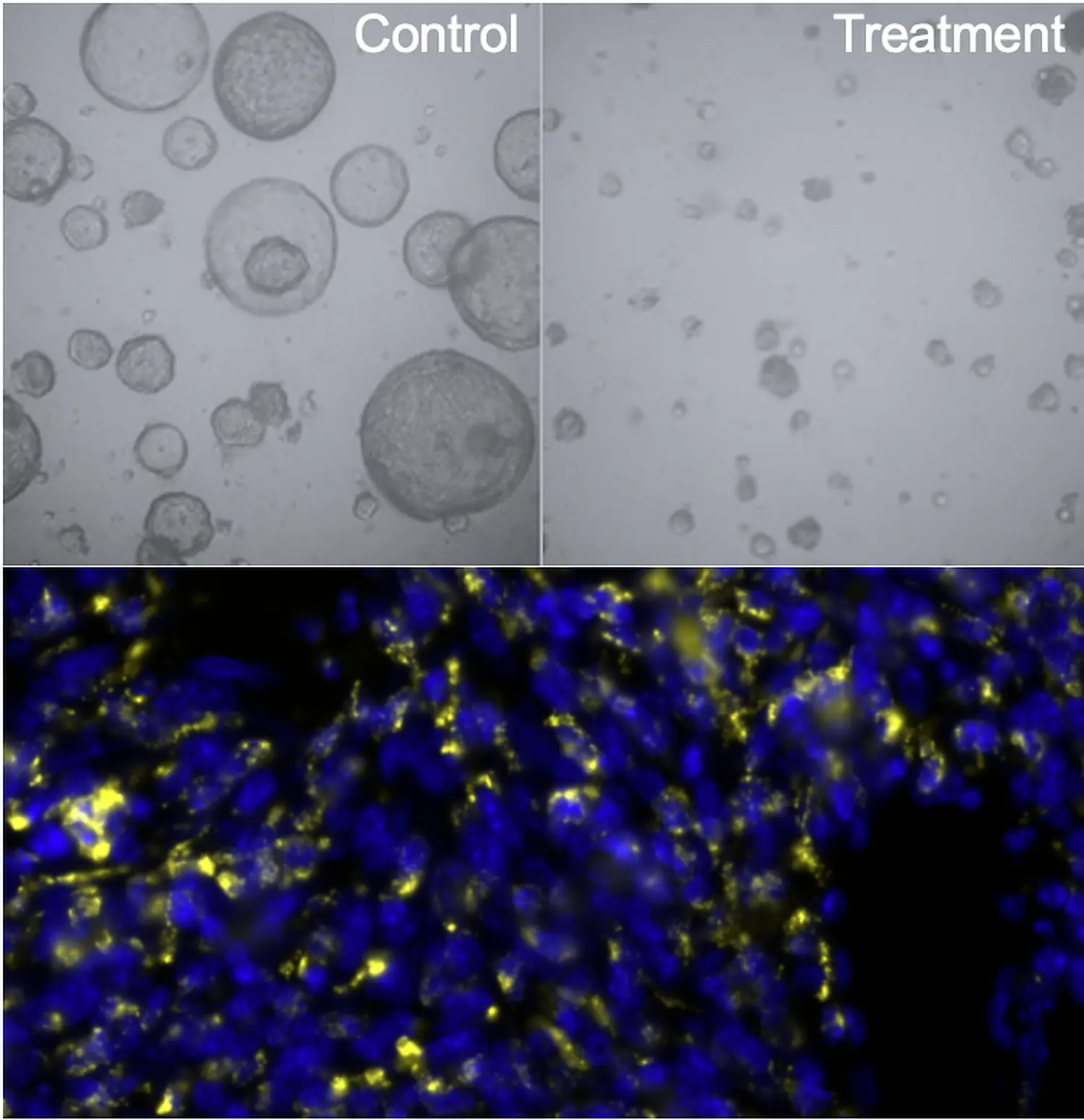
© umg/constanza tapia contreras und gsh/zuzana tatarova
Neue Erkenntnisse: Zwei Schwachstellen gleichzeitig angreifen
Das Pankreaskarzinom zeichnet sich durch eine besonders hohe Widerstandsfähigkeit gegenüber gängigen Therapien aus. Selbst neue zielgerichtete Medikamente, die bestimmte Krebs-Gene blockieren, verlieren oft rasch ihre Wirkung, weil Tumorzellen Ausweichstrategien entwickeln. Der PI3K-Signalweg spielt eine zentrale Rolle bei der Entstehung und dem Fortschreiten von Bauchspeicheldrüsenkrebs. Bisherige Versuche, diesen Weg therapeutisch zu blockieren, waren jedoch wenig erfolgreich. Die Göttinger Forschenden entdeckten nun, dass Krebszellen auf die Blockade des PI3K-Signalwegs mit der verstärkten Aktivierung eines anderen zellulären Mechanismus reagieren: der SUMOylierung. Bei diesem Prozess werden kleine Proteine, sogenannte SUMO-Proteine, an bestimmte Zielproteine angehängt, wodurch dessen Funktion und Stabilität verändert wird und den Krebszellen hilft, sich an Stress anzupassen.
„Wir konnten erstmals zeigen, dass die beiden Signalwege wechselseitig voneinander abhängig sind. Blockiert man einen Weg, aktivieren die Krebszellen den anderen als Kompensation“, erklärt Prof. Dr. Keller, Letztautor der Studie.
„Die Kombinationstherapie wirkt auf mehreren Ebenen. Sie tötet nicht nur die Krebszellen direkt ab, sondern aktiviert auch das Immunsystem. Die Abwehrzellen konnten besser in den Tumor eindringen und die Krebszellen bekämpfen. Diese doppelte Wirkung der direkten Krebszellabtötung und der Aktivierung der körpereigenen Abwehr macht den Ansatz besonders vielversprechend“, ergänzt Priv.-Doz. Dr. Matthias Wirth, Letztautor der Studie.
Bedeutender Therapieansatz für Patient*innen
Um einen neuen Therapieansatz zu entwickeln, müssen die Ergebnisse in weiteren Studien untersucht werden.
„Unsere Ergebnisse zeigen, dass die gleichzeitige Hemmung von PI3K und SUMO eine bislang ungenutzte Schwachstelle des Bauchspeicheldrüsenkrebses aufdeckt“
Priv.-Doz. Dr. Matthias Wirth
Originialpublikation: Köse Hazal, Schneeweis Christian, Putze Philipp et al. Targeting mutual dependence of PI3Kα/δ and SUMO signaling in pancreatic cancer Gastroenterology 2025
Quelle: Pressemitteilung Universitätsmedizin Göttingen