Forschende am Universitätsklinikum Tübingen haben eine neue Schwachstelle im Erbgut von Medulloblastomen bei Kindern entdeckt. Mithilfe der CRISPR-Genschere identifizierten sie das Gen DNMT1 als vielversprechenden Therapieansatz. Die Kombination von DNMT1- und SHH-Inhibitoren zeigte in Modellen einen deutlichen Behandlungserfolg – unterstützt von der Wilhelm-Sander-Stiftung.
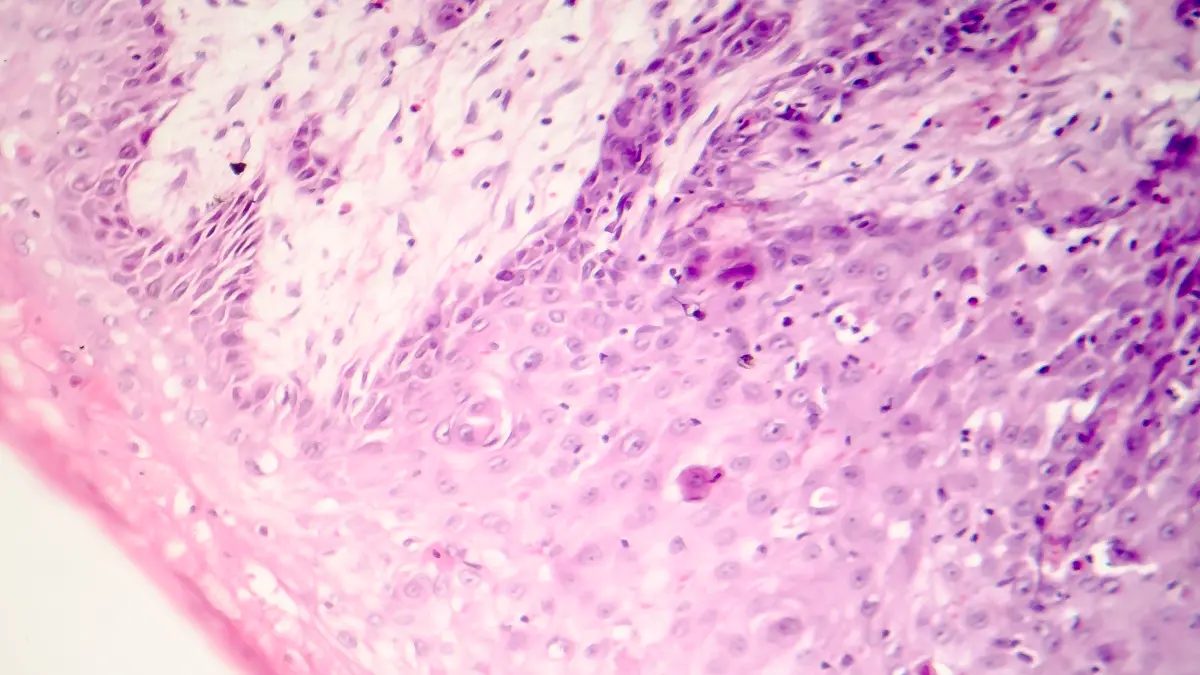
Hirntumore sind nach den Leukämien die zweithäufigsten Krebserkrankungen im Kindesalter. Das Medulloblastom, eine aggressive Form von Hirntumoren, entsteht im Bereich des Kleinhirns, das unter anderem für die Bewegungskoordination verantwortlich ist. Neueste molekulargenetische Untersuchungen am Erbgut dieser Tumore konnten zeigen, dass es sich hierbei tatsächlich um vier unterschiedliche Krebserkrankungen handelt. Eine Untergruppe der Medulloblastome zeigt eine hohe Aktivität des Sonic Hedgehog (SHH)-Signalwegs. Diese Tumore können bei Erwachsenen durch den Einsatz von SHH-Inhibitoren, also Hemmstoffen, bereits behandelt werden. Da der SHH-Signalweg während der kindlichen Entwicklung in unterschiedlichen Geweben eine wichtige Rolle spielt, können diese Medikamente bei der Behandlung von Kindern aufgrund einer Vielzahl systemischer Nebenwirkungen jedoch nicht zum Einsatz kommen. Neue zielgerichtete Therapien für das SHH-Medulloblastom werden daher dringend benötigt, um vor allem den jüngsten Patienten eine schonendere und effektivere Behandlung zu ermöglichen.
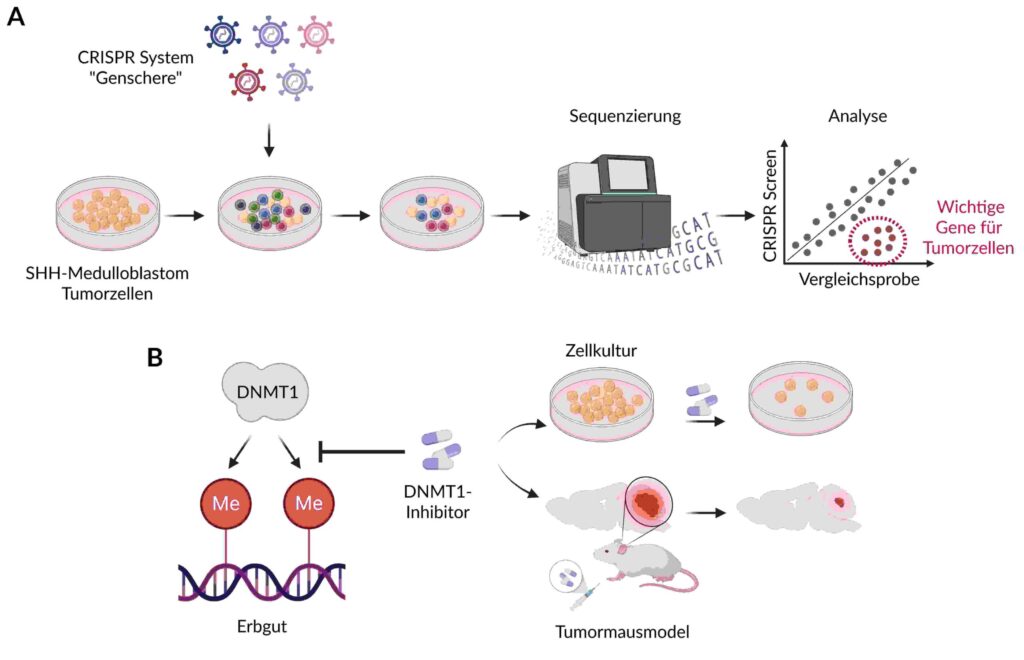
CRISPR-Genschere identifiziert Schwachstellen im Tumor
Das Team um Daniel Merk am Hertie-Institut für klinische Hirnforschung in Tübingen nutzt neuartige molekulargenetische Untersuchungen, um Schwachstellen im Erbgut von Tumoren zu identifizieren, die als Ansatzpunkt für neuartige Therapieverfahren dienen können. Eines der wichtigsten Werkzeuge ist die CRISPR-Genschere, mit deren Hilfe sich alle Gene im Erbgut einer Tumorzelle ausschalten lassen. In geeigneten Modellsystemen können die Forschenden mithilfe von CRISPR schnell eine Aussage darüber treffen, welche Gene für einen Tumor besonders wichtig sind. „Mit Hilfe dieser Technologie können wir direkt verfolgen, was passiert, wenn wir dem Tumor ein Gen nach dem anderen wegnehmen“, erklärt Studienleiter Daniel Merk. „Somit können wir direkt priorisieren, welche Gene vermutlich ein lohnenswerter Ansatzpunkt für neuartige Therapien sind.“
Epigenetische Regulatoren als Schlüssel zum Erfolg
Die Ergebnisse zeigen, dass Tumorzellen aus SHH-Medulloblastomen besonders abhängig sind von sogenannten epigenetischen Regulatoren – das sind molekulare Werkzeuge der Zelle, die die Verpackung des Erbguts kontrollieren und somit einen direkten Einfluss darauf haben, wie sich die Tumorzellen verhalten. Manche dieser Regulatoren, wie etwa das Gen DNMT1, können durch Medikamente in ihrer Funktion eingeschränkt und somit inhibiert werden.
Die Analyse von Tumormaterial von Patienten mit einem SHH-Medulloblastom zeigt, dass das Gen DNMT1 einen direkten Einfluss auf den Krankheitsverlauf hat: Je aktiver DNMT1 in den Tumoren ist, desto geringer sind die Heilungschancen. Weitere Untersuchungen im Labor liefern dafür eine Erklärung. Obwohl DNMT1 kein direkter Teil des SHH-Signalwegs ist, spielt es in der Signalübertragung dennoch eine wichtige Rolle – schaltet man DNMT1 ab, wird auch der SHH-Signalweg gestört.
Kombinationstherapie zeigt vielversprechende Ergebnisse
Zur weiteren Untersuchung haben die Forscher in Tierversuchen mit Mäusen gearbeitet, die genetisch so verändert wurden, dass sie ein SHH-Medulloblastom entwickeln. Tatsächlich hemmen sowohl SHH-Inhibitoren als auch DNMT1-Inhibitoren das Wachstum der Tumore. Das Überraschende: Mäuse, die beide Medikamente erhielten, zeigten den größten Behandlungserfolg. Dieser synergistische Effekt beider Medikamente konnte von den Krebsforschern auch in speziellen Kulturen von humanen SHH-Medulloblastomen nachgewiesen werden.
DNMT1-Inhibitoren werden bereits in der Klinik zur Behandlung bestimmter Leukämien bei Kindern angewendet und zeigen im Gegensatz zu SHH-Inhibitoren bei jungen Patienten keine gravierenden Nebenwirkungen. Die Krebsforscher hoffen daher, dass ihre Ergebnisse einen neuen Ansatzpunkt zur Behandlung der jüngsten Patienten mit SHH-Medulloblastomen bieten. Auch ältere Patienten, bei denen SHH-Inhibitoren sicher angewendet werden können, könnten in Zukunft von einer möglichen Kombinationstherapie beider Medikamente profitieren.
Originalpubliaktion:
- Tsiami F, Lago C, Pozza N et al. Genome-wide CRISPR-Cas9 knockout screens identify DNMT1 as a druggable dependency in sonic hedgehog medulloblastoma Acta Neuropathologica Communications 2024; 12: 125
- Tsiami F, Drwesh L, Surender S et al. SMARCA5 is required for the development of granule cell neuron precursors and Sonic Hedgehog Medulloblastoma growth Scientific Reports 2025; 15: 26091
Quelle: Pressemitteilung Wilhelm Sander-Stiftung
Bildquelle: © pikovit – stock.adobe.com