Glioblastome gehören zu den therapieresistentesten malignen Hirntumoren. Neue immuntherapeutische Ansätze, die gezielt die Tumorheterogenität adressieren, könnten die Behandlungsmöglichkeiten entscheidend erweitern.
Zielantigene und duale CAR-T-Zell-Strategie
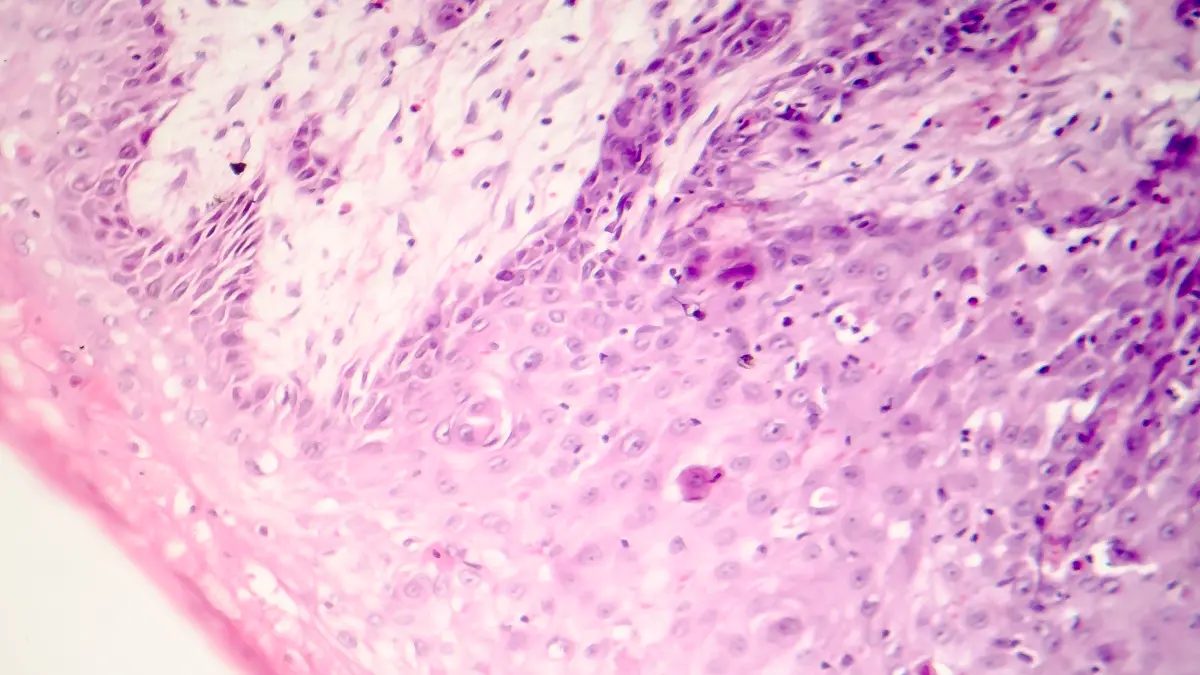
Die ausgeprägte inter- und intratumorale Heterogenität des Glioblastoms erschwert den Erfolg herkömmlicher CAR-T-Zelltherapien. In dieser beim DGHO präsentierten Studie wurden die Zielantigene Podoplanin (PDPN) und GD2 in primären sowie rezidivierenden Glioblastomen systematisch identifiziert und charakterisiert. Darauf aufbauend kamen duale CAR-T-Zellen zum Einsatz, die beide Antigene simultan adressieren und somit eine breitere Wirksamkeit gegen heterogene Tumorzellpopulationen ermöglichen.
Überlegenheit der dualen Therapie in präklinischen Modellen
Die dual-targeting CAR-T-Zellen wurden in einem umfassenden präklinischen Setting getestet, das sowohl Glioblastom-Zelllinien als auch patientenabgeleitete Organoide und orthotope Mausmodelle umfasste. Im Vergleich zu monospezifischen CAR-T-Zellen zeigten die dualen Zellprodukte eine signifikant gesteigerte Apoptoseinduktion und Zytotoxizität sowie eine effiziente Tumorregression in vivo. Darüber hinaus führte die duale Therapie zu einer deutlichen Verlängerung des Gesamtüberlebens und in einzelnen Fällen sogar zur Heilung in Mausmodellen.
Diese Ergebnisse weisen darauf hin, dass PDPN/GD2-duale CAR-T-Zellen einen vielversprechenden Ansatz darstellen, um die therapeutischen Limitationen bei Glioblastomen zu überwinden und neue Behandlungsoptionen für diese bislang unheilbare Erkrankung zu schaffen.
Quelle: Hübner J et al. PDPN/GD2-CAR T cells as an innovative dual therapy approach for the treatment of glioblastoma. Jahrestagung der Deutschen, Österreichischen und Schweizerischen Gesellschaften für Hämatologie und Medizinische Onkologie 24.–27. Oktober 2025, Köln