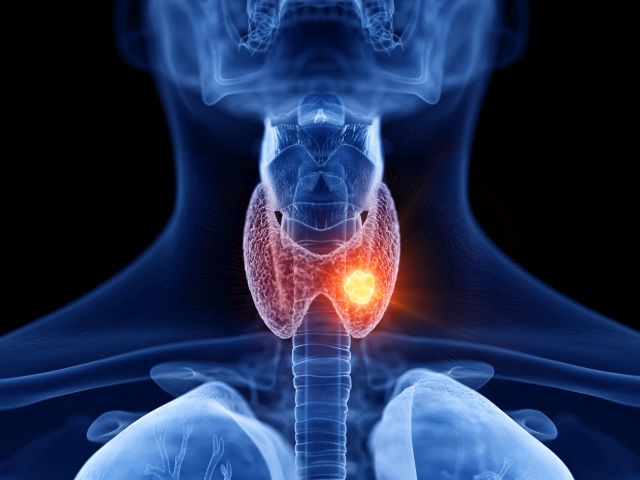
Forschende der Cell Biology Unit der Universitätsmedizin Mainz haben eine weitere Ursache für das sogenannte papilläre Schilddrüsenkarzinom (PTC) identifiziert: eine bislang unbekannte Kombination zweier Proteine, die das Tumorwachstum in der Schilddrüse fördert. Diese neu entdeckte Verbindung entsteht durch genetische Veränderungen körpereigener Zellen. Den Mainzer Wissenschaftlern gelang es, die krebsfördernde Funktion dieser Proteinfusion mit bereits bekannten onkologischen Wirkstoffen zu hemmen. Aus dieser Erkenntnis lassen sich personalisierte Therapieansätze für Menschen entwickeln, die diese krebserregende Proteinverbindung in sich tragen. Nachzulesen sind die Studienergebnisse in der renommierten Fachzeitschrift „Molecular Cancer“.
„Da Krebszellen aus körpereigenen, sich genetisch verändernden Zellen entstehen, kann PTC bei jedem Patienten in einer anderen genetischen Veränderung begründet sein. Das Ziel unseres Forschungsprojekts war es, sogenannte Onkogene zu identifizieren, aus denen krebserregende Proteine entstehen“, erläutert der Leiter der Cell Biology Unit der Universitätsmedizin Mainz, Univ.-Prof. Dr. Krishnaraj Rajalingam.
Die Forschenden um Professor Rajalingam untersuchten in ihrer Studie zunächst das Tumorgewebe einer PTC-Patientin, die zudem unter der chronischen Schilddrüsenentzündung Hashimoto-Thyroiditis litt. Um mehr über den spezifischen Tumor zu erfahren, führten die Wissenschaftler eine sogenannte Multiomik-Analyse durch, bei der unter anderem die RNA-Sequenzierung eingesetzt wird.
Proteinfusion als Ursprung des PTC
Dem Forschungsteam gelang es, ein bisher unbekanntes Fusionsprotein zu isolieren: eine Verbindung des häufig mutierten und krebsfördernden Onkogens BRAF mit dem Protein BAIAP2L1, das die Neubildung von Blutgefäßen reguliert. Durch den Einsatz des bereits aus der Onkologie bekannten Wirkstoffes PLX8394, vermochten sie darüber hinaus, die krebsfördernde Proteinfusion BAIAP2L1-BRAF zu hemmen.
Das Team der Cell Biology Unit untersuchte zudem das Tumorgewebe von weiteren PTC-Betroffenen. Es identifizierte sowohl bereits bekannte krebsfördernde Fusionsproteine als auch weitere Faktoren, die zum Tumorwachstum beitragen und somit Zielstrukturen für therapeutische Maßnahmen darstellen. Mit sogenannten Gen Knock-Downs konnten die Forschenden zunächst bestätigen, dass die identifizierten Faktoren für die Tumorbildung relevant sind. Darüber hinaus stellten sie fest, dass bei den PTC-Betroffenen, die Zielstrukturen in auffällig hoher beziehungsweise niedriger Konzentration vorhanden waren, und zwar unabhängig davon, welche Mutationen vorlagen. Die eingesetzten Wirkstoffe erzielten also das gewünschte Resultat, ganz gleich sich das BAIAP2L1-BRAF-Fusionsprotein gebildet hatte oder andere genetische Veränderungen existierten.
Ein weiterer Schritt zu personalisierten Therapeutika
Die Mainzer Studie belegt, wie die integrative Analyse von Patientenmaterial die Präzisionsmedizin und personalisierte Therapeutika voranbringen kann, indem sie sowohl patientenspezifische als auch patientenübergreifende Zielstrukturen identifiziert und klassifiziert. Die Universitätsmedizin Mainz, als translationale Forschungseinrichtung und Haus der Supramaximalversorgung, arbeitet intensiv daran, ihr Angebot hinsichtlich der Personalisierten Medizin weiter zu stärken. Dabei wird sie auf ihre jahrzehntelange immunologische Tradition, zahlreiche herausragenden Forschungserfolge sowie Beteiligungen, wie beispielsweise an TRON – Translationale Onkologie an der Universitätsmedizin der Johannes Gutenberg-Universität Mainz, und Kooperationen zurückgreifen.
Originalpublikation: Renaud E et al. Multiomic analysis of papillary thyroid cancers identifies BAIAP2L1-BRAF fusion and requirement of TRIM25, PDE5A and PKCδ for tumorgenesis. Mol Cancer 2022; 21(1): 1–15
Quelle: Pressemitteilung der Universitätsmedizin der Johannes Gutenberg-Universität Mainz
Bilderquelle: © SciePro – stock.adobe.com